Es ist bekannt, dass Intervallfasten* die Empfindlichkeit für das blutzuckersenkende Hormon Insulin verbessert und vor einer Fettleber schützt. DZD-Wissenschaftlerinnen und -Wissenschaftler vom DIfE fanden nun heraus, dass bei Mäusen, die eine Intervallfasten-Kur bekamen, auch das Fett der Bauchspeicheldrüse schrumpfte. In ihrer neuen Arbeit im Fachblatt Metabolism zeigen sie, über welchen Mechanismus das Bauchspeicheldrüsenfett zur Entwicklung eines Typ-2-Diabetes beitragen könnte.
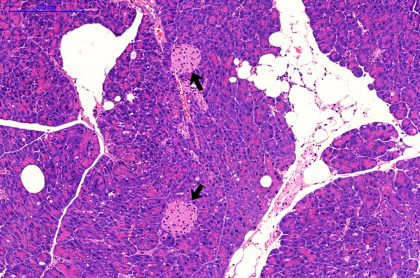
Als bekannte und häufig vorkommende Krankheit ist die Fettleber gründlich erforscht. Über die durch Übergewicht entstehende Fettansammlung in der Bauchspeicheldrüse und deren Auswirkungen auf den Ausbruch von Typ-2-Diabetes ist jedoch wenig bekannt. Das Forscherteam um Professorin Annette Schürmann und Professor Tim J. Schulz vom Deutschen Institut für Ernährungsforschung (DIfE) fand nun heraus, dass übergewichtige Mäuse, die anfällig für Diabetes sind, eine hohe Ansammlung an Fettzellen in der Bauchspeicheldrüse aufwiesen. Mäuse, die trotz eines hohen Gewichts aufgrund ihres Erbguts gegen Diabetes gefeit sind, hatten hingegen kaum Fett in der Bauchspeicheldrüse, dafür aber in der Leber.
„Fettansammlungen außerhalb des Fettgewebes, z.B. in Leber, Muskeln oder gar den Knochen, wirken sich negativ auf diese Organe und den gesamten Körper aus. Welchen Einfluss Fettzellen innerhalb der Bauchspeicheldrüse haben, war bisher nicht klar“, erklärt Schürmann, Leiterin der Abteilung Experimentelle Diabetologie am DIfE und Sprecherin des Deutschen Zentrums für Diabetesforschung (DZD).
Intervallfasten lässt Fett der Bauchspeicheldrüse schmelzen
Das Wissenschaftlerteam teilte die dicken, für Diabetes anfälligen Tiere in zwei Gruppen: Die erste Gruppe durfte so viel fressen, wie sie wollte. Die zweite Gruppe erhielt eine Intervallfasten-Kur: einen Tag bekamen die Nager unbegrenzt Futter und am nächsten Tag bekamen sie nichts. Nach fünf Wochen konnten die Forscherinnen und Forscher Unterschiede in den Bauchspeicheldrüsen der Mäuse sehen: In der Gruppe eins reicherten sich Fettzellen an. Die Tiere der Gruppe zwei hatten hingegen kaum Fetteinlagerungen in der Bauchspeicheldrüse.
Fettzellen stimulieren Ausschüttung von Insulin
Um herauszufinden, wie Fettzellen die Funktion der Bauchspeicheldrüse beeinträchtigen könnten, isolierten die Wissenschaftlerinnen und Wissenschaftler um Schürmann und Schulz erstmals Fett-Vorläuferzellen aus der Bauchspeicheldrüse von Mäusen und ließen sie zu reifen Fettzellen ausdifferenzieren. Wurden die reifen Fettzellen anschließend zusammen mit den Langerhans-Inseln** der Bauchspeicheldrüse kultiviert, setzten die Beta-Zellen der „Inseln“ verstärkt Insulin frei.
„Wir vermuten, dass durch die erhöhte Insulinfreisetzung die Langerhans-Inseln von diabetesanfälligen Tieren schneller erschöpfen und nach einiger Zeit ihre Funktion ganz einstellen. Auf diese Weise könnte Fett in der Bauchspeicheldrüse zur Entstehung des Typ-2-Diabetes beitragen“, sagt Schürmann.
Bedeutung des Bauchspeicheldrüsenfetts für die Diabetesprävention
Die aktuellen Daten lassen vermuten, dass zur Vorbeugung eines Typ-2-Diabetes nicht nur das Leberfett gesenkt werden sollte. „Möglicherweise trägt gerade die Fettansammlung in der Bauchspeicheldrüse unter bestimmten genetischen Voraussetzungen entscheidend zur Entwicklung eines Typ-2-Diabetes bei“, sagt Schulz, Leiter der Abteilung Fettzell-Entwicklung und Ernährung. Als vielversprechender Therapieansatz könnte zukünftig Intervallfasten zum Einsatz kommen. Die Vorteile: Es ist nicht-invasiv, lässt sich meist leicht in den Alltag integrieren und kommt ohne Medikamente aus.
*) Intervallfasten – auch als intermittierendes Fasten bekannt – bedeutet, in bestimmten Zeitfenstern auf Nahrung zu verzichten. Wasser, ungesüßter Tee und schwarzer Kaffee sind rund um die Uhr erlaubt. Je nach Methode dauern die Essenspausen zwischen 16 und 24 Stunden oder es werden innerhalb einer Woche an zwei Tagen höchstens 500 bis 600 Kalorien aufgenommen. Die bekannteste Form des Intervallfastens ist die 16:8-Methode: An acht Stunden des Tages darf gegessen werden und die übrigen 16 Stunden wird gefastet. Eine Mahlzeit – meist das Frühstück – wird dabei ausgelassen.
**) Die Langerhans-Inseln – auch als Inselzellen oder Langerhans‘sche Inseln bezeichnet – sind inselartig eingebettete Ansammlungen hormonbildender Zellen in der Bauchspeicheldrüse. Ein gesunder Erwachsener hat etwa eine Millionen Langerhans-Inseln. Jede „Insel“ hat einen Durchmesser von 0,2-0,5 Millimeter. Die Beta-Zellen stellen das blutzuckersenkende Hormon Insulin her und machen etwa 65 bis 80 Prozent der Inselzellen aus. Sie geben bei erhöhten Blutzuckerspiegeln Insulin ins Blut ab, damit sich diese wieder normalisieren.
Literatur:
Original-Publikation: Quiclet, C., Dittberner, N., Gässler, A., Stadion, M., Gerst, F., Helms, A., Baumeier, C., Schulz, T. J., Schürmann, A.: Pancreatic adipocytes mediate hypersecretion of insulin in diabetes-susceptible mice. Metabolism. 97, 9-17 (2019). [https://doi.org/10.1016/j.metabol.2019.05.005]
Ähnlicher Artikel: Baumeier, C., Kaiser, D., Heeren, J., Scheja, L., John, C., Weise, C., Eravci, M., Lagerpusch, M., Schulze, G., Joost, H.-G., Schwenk, R. W., Schürmann, A.: Caloric restriction and intermittent fasting alter hepatic lipid droplet proteome and diacylglycerol species and prevent diabetes in NZO mice. Biochim. Biophys. Acta/Mol. Cell Biol. Lipids 1851, 566-576 (Open Access) (2015). [https://doi.org/10.1016/j.bbalip.2015.01.013]
Hintergrundinformationen
Deutsches Institut für Ernährungsforschung Potsdam-Rehbrücke (DIfE)
Das DIfE ist Mitglied der Leibniz-Gemeinschaft. Es erforscht die Ursachen ernährungsassoziierter Erkrankungen, um neue Strategien für Prävention, Therapie und Ernährungsempfehlungen zu entwickeln. Zu seinen Forschungsschwerpunkten gehören die Ursachen und Folgen des metabolischen Syndroms, einer Kombination aus Adipositas (Fettsucht), Hypertonie (Bluthochdruck), Insulinresistenz und Fettstoffwechselstörung, die Rolle der Ernährung für ein gesundes Altern sowie die biologischen Grundlagen von Nahrungsauswahl und Ernährungsverhalten. Das DIfE ist zudem ein Partner des 2009 vom BMBF geförderten Deutschen Zentrums für Diabetesforschung (DZD).
Deutsches Zentrum für Diabetesforschung e.V. (DZD)
Das DZD ist eines der sechs Deutschen Zentren der Gesundheitsforschung. Es bündelt Experten auf dem Gebiet der Diabetesforschung und verzahnt Grundlagenforschung, Epidemiologie und klinische Anwendung. Ziel des DZD ist es, über einen neuartigen, integrativen Forschungsansatz einen wesentlichen Beitrag zur erfolgreichen, maßgeschneiderten Prävention, Diagnose und Therapie des Diabetes mellitus zu leisten.
Mitglieder des Verbunds sind das Helmholtz Zentrum München – Deutsches Forschungszentrum für Gesundheit und Umwelt, das Deutsche Diabetes-Zentrum (DDZ) in Düsseldorf, das Deutsche Institut für Ernährungsforschung (DIfE) in Potsdam-Rehbrücke, das Institut für Diabetesforschung und Metabolische Erkrankungen des Helmholtz Zentrum München an der Eberhard-Karls-Universität Tübingen und das Paul-Langerhans-Institut Dresden des Helmholtz Zentrum München am Universitätsklinikum Carl Gustav Carus der TU Dresden, assoziierte Partner an den Universitäten in Heidelberg, Köln, Leipzig, Lübeck und München sowie weitere Projektpartner.
Pressekontakte:
Prof. Dr. Annette Schürmann
Abteilung Experimentelle Diabetologie
Deutsches Institut für Ernährungsforschung Potsdam-Rehbrücke (DIfE)
Tel.: +49 (0)33200 88-2368
E-Mail: schuermann@dife.de
Sonja Schäche
Referentin für Presse- und Öffentlichkeitsarbeit
Deutsches Institut für Ernährungsforschung Potsdam-Rehbrücke (DIfE)
Tel.: +49 33200 88-2278
E-Mail: sonja.schaeche@dife.de / presse@dife.de
++ Helfen Sie mit, die Diabetesprävention in Deutschland zu verbessern! Unterstützen Sie unsere Wissenschaftler bei ihrem Citizen Science-Projekt DIRIKO: https://diriko.dife.de/ – Vielen Dank! ++
Quelle: DIfE
